Los modelos atómicos
Los
Modelos Atómicos son representaciones del átomo para intentar dar una
explicación de su estructura. De un modelo planteado, se deducen sus
propiedades, que luego deberán corroborarse experimentalmente. La materia está
compuesta por partículas muy pequeñas a las que llamamos átomos. Los átomos
tienen características y propiedades determinadas
Al
tratarse de partículas tan pequeñas, hace muchos años, era muy difícil poder
explicar cómo estaban formados los átomos, sin embargo gracias a los avances
tecnológicos hemos avanzado en el conocimiento del átomo y que lo conforma; a
lo largo de nuestra historia se han elaborado diferentes Modelos Atómicos que
tienen el nombre del científico que lo ideó. Estos Modelos Atómicos se fueron
descartando, mejorando y planteando nuevos, hasta llegar al Modelo Atómico
actual. Aquí te explicare la evolución histórica de los
Modelos Atómicos.
Modelo
Atómico de Demócrito
Demócrito,
un filósofo griego, aproximadamente en el 450 a.C., desarrolló la “teoría atómica del universo”,
que fue concebida por su mentor, el filósofo Leucipo.
Esta
teoría, no se apoya en resultados experimentales sino que se desarrolla
mediante razonamientos lógicos, por ser una teoría filosófica. Puede enunciarse
de la siguiente manera:
Los
átomos se diferencian solo en forma y tamaño, pero no por cualidades internas.
Las
propiedades de la materia varían según el agrupamiento de los átomos.
Además,
afirma que toda la materia es una mezcla de elementos originarios que poseen
las características de inmutabilidad y eternidad, concebidos como entidades infinitamente
pequeñas y, por tanto, imperceptibles para los sentidos, a las que Demócrito
llamó átomos, que en griego significa “indivisible”.
Modelo
Atómico de Dalton
Fue
desarrollado a principios de 1800 (se estima, entre 1803 y 1807) por el
científico británico John Dalton. Fue el primer modelo atómico con bases
científicas.
Su
modelo atómico (Dalton lo llamó “Teoría Atómica”) consta de los siguientes
enunciados:
La
materia está formada por partículas muy pequeñas llamadas átomos, que son
indivisibles y no se pueden destruir.
Los átomos de un mismo elemento son iguales entre sí, tienen la misma masa e iguales propiedades. Los átomos de diferentes elementos tienen masa diferente. Comparando la masa de los elementos con los del hidrógeno tomado como la unidad, propuso el concepto de peso atómico relativo.
Los átomos permanecen sin división, aun cuando se combinen en las reacciones químicas.
Los átomos, al combinarse para formar compuestos, guardan relaciones simples de números enteros y pequeños.
Los átomos de elementos diferentes se pueden combinar en proporciones distintas y formar más de un compuesto.
Los compuestos químicos se forman al unirse átomos de dos o más elementos.
Más adelante se encontraron insuficiencias al modelo atómico de Dalton:
Los átomos están formados por partículas subatómicas y son divisibles.
Existen átomos del mismo elemento con diferente masa (Isótopos).
Existen moléculas formadas por 2 o más átomos del mismo elemento (Por ejemplo O2; H2, etc.).
Los átomos de un mismo elemento son iguales entre sí, tienen la misma masa e iguales propiedades. Los átomos de diferentes elementos tienen masa diferente. Comparando la masa de los elementos con los del hidrógeno tomado como la unidad, propuso el concepto de peso atómico relativo.
Los átomos permanecen sin división, aun cuando se combinen en las reacciones químicas.
Los átomos, al combinarse para formar compuestos, guardan relaciones simples de números enteros y pequeños.
Los átomos de elementos diferentes se pueden combinar en proporciones distintas y formar más de un compuesto.
Los compuestos químicos se forman al unirse átomos de dos o más elementos.
Más adelante se encontraron insuficiencias al modelo atómico de Dalton:
Los átomos están formados por partículas subatómicas y son divisibles.
Existen átomos del mismo elemento con diferente masa (Isótopos).
Existen moléculas formadas por 2 o más átomos del mismo elemento (Por ejemplo O2; H2, etc.).
Modelo
Atómico de Lewis: Modelo atómico cúbico
Esta
teoría se desarrolló en 1902 por G. Lewis, pero fue publicada en 1916 en el
artículo “The Atom and the Molecule” (El átomo y la molécula).
El
modelo atómico de Lewis representa al átomo como un cubo, donde los electrones
estaban colocados en cada uno de los 8 vértices de ese cubo.
El
Modelo Atómico Cúbico representó un paso importante hacia el entendimiento del
enlace químico, ya que introdujo el concepto de “valencia de un átomo”, es
decir, la cantidad de electrones en el último nivel de energía del átomo que se
pondrán en juego en un enlace químico. El artículo de 1916 de Lewis también
introdujo el concepto del par de electrones en el enlace covalente, la regla
del octeto, y la ahora llamada estructura de Lewis.
El
modelo del átomo cúbico se abandonó pronto y es, por tanto, sólo de interés
histórico.
Modelo
Atómico de Thomson (o Pudín de Pasas)
Fue
desarrollado en 1906 por el científico británico Joseph John “J.J.” Thomson,
quien unos años antes había descubierto el electrón.
En
este modelo, el átomo está compuesto por electrones de carga negativa en un
átomo de carga positiva. Los electrones se hallan incrustados en este al igual
que las pasas de un pudín (o budín). Por esta analogía también se lo denomina
“Modelo del pudín de pasas”. Los electrones se distribuyen uniformemente en el
interior del átomo, suspendidos en una nube de carga positiva. El átomo se
considera como una esfera con carga positiva con electrones repartidos como
pequeños gránulos.
La
herramienta principal con la que contó Thomson para su modelo atómico fue la
electricidad.
Modelo
atómico de Rutherford (o Modelo Planetario)
Este
modelo fue propuesto en 1911 por el químico y físico británico-neozelandés
Ernest Rutherford. Este científico había desarrollado un experimento denominado
“experimento de la lámina de oro” el cual le permitió enunciar el modelo
atómico. Fue el primer modelo en separar
al átomo en dos zonas: núcleo y corteza. A partir de aquí, se empezaron a
estudiar por separado.
Según
este modelo:
El
átomo consta de un núcleo central donde se concentra la carga positiva y casi
toda la masa. Este núcleo es muy pequeño comparado con el tamaño total.
El
átomo posee electrones, de carga negativa que se sitúan en la corteza, describiendo
órbitas circulares y girando a gran velocidad, como un sistema planetario.
La
suma de las cargas negativas de los electrones debe ser igual a la carga
positiva del núcleo, siempre que el átomo sea neutro.
Modelo
atómico de Bohr
Fue
postulado en 1913 por el físico danés Niels Bohr. Puede considerarse
transicional ya que se ubica entre la mecánica clásica y la cuántica. Incorpora
ideas tomadas del efecto fotoeléctrico, explicado por Einstein. A partir de la
idea de que en un átomo los electrones giran alrededor del núcleo, Bohr propuso
5 postulados:
El
electrón sólo puede moverse a cierta distancia (radio) del núcleo, lo que
determina una órbita o nivel de energía (también se lo llama capa). Una órbita
es una trayectoria circular bien definida alrededor del núcleo.
Mientras
se encuentre en una órbita, el electrón no libera ni absorbe energía; por esto
se conoce a las órbitas como estacionarias (o permitidas). En una órbita, la
energía permanece constante.
Cuando
se le entrega energía a un átomo, el electrón puede absorberla y pasar a una
órbita de mayor radio y mayor energía. En este caso, se dice que el electrón
está en estado excitado. Cuando los electrones de un átomo no están excitados,
el átomo se encuentra en estado fundamental.
Cuando
un electrón pasa de una órbita más alejada del núcleo a otra más cercana
entonces libera o emite energía en forma de fotón (una cantidad pequeña y
determinada de energía).
Para
pasar de una órbita a otra, el electrón debe absorber o emitir una cantidad de
energía igual a la diferencia de energía entre un nivel y el otro (esto es
porque la energía no se destruye, sino que se transforma). Si pasa de un nivel
inicial (con una cantidad de energía Ei) a otro final (con otra cantidad de
energía Ef.). A las órbitas se las designa con el número cuántico n, que toma
los valores: 1, 2, 3, 4, 5, 6 y 7. Cuanto más alejada del núcleo, más energía
tiene la órbita.
Modelo
atómico de Sommerfeld
Fue
desarrollado en 1916 por el físico alemán Arnold Sommerfeld, basándose en la
teoría de la relatividad de Albert Einstein, por lo que se dice que es un
modelo atómico relativista.
Hizo
modificaciones al modelo de Bohr. Aun así, sigue siendo válido para el átomo de
Hidrógeno, pero al tratar de explicar el comportamiento de átomos de otros
elementos, presenta insuficiencias.
El
modelo atómico de Sommerfeld postula que:
Los
electrones se mueven alrededor del núcleo, en órbitas circulares o elípticas.
A
partir del segundo nivel energético existen dos o más subniveles en el mismo
nivel
El
electrón es una corriente eléctrica minúscula.
El
núcleo atómico, al igual que los electrones, se mueven alrededor de un centro
de masas del sistema.
Ese
centro de masa estará muy cercano al núcleo ya que su masa es muy superior a la
masa de los electrones
Esta
modificación la introdujo para justificar los valores de frecuencias halladas
experimentalmente (en relación a las calculadas teóricamente).
Modelo
atómico de Schrödinger
Fue
desarrollado en 1926 por el físico y filósofo austríaco Erwin Rudolf Josef
Alexander Schrödinger. Es un modelo cuántico no relativista.
Tiene
las siguientes características:
Describe
el movimiento de los electrones como ondas estacionarias.
Postula
que los electrones se mueven constantemente, es decir, no tienen una posición
fija o definida dentro del átomo.
Establece
una zona de probabilidad para ubicar al electrón, no predice la ubicación del
electrón.
Las
áreas de probabilidad donde se hallaría el electrón se denominan orbitales
atómicos. Los orbitales describen un movimiento de traslación alrededor del
núcleo del átomo.
Estos
orbitales atómicos tienen diferentes niveles y subniveles de energía, y pueden
definirse entre nubes de electrones.
El
modelo no contempla la estabilidad del núcleo, sólo se remite a explicar la
mecánica cuántica asociada al movimiento de los electrones dentro del átomo.
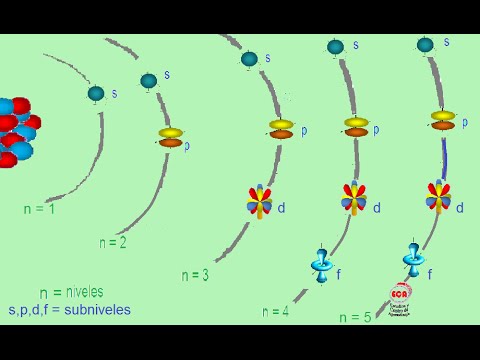
Modelo
atómico Actual o Modelo Orbital
Este
modelo atómico se desarrolló en la década de 1920, como resultado del aporte de
conocimientos de muchos científicos, entre ellos Broglie, Einstein, Bohr,
Schrödinger, Heisenberg.
Está
basado en la mecánica cuántica ondulatoria, la cual está fundamentada en los
números cuánticos.
Los
números cuánticos son 4: n, l, m, s. Sirven para describir cada uno de los
electrones de un átomo. Cabe destacar que, para los electrones de un mismo
átomo, la combinación de estos 4 números nunca es la misma.
En
esta teoría se afirma que:
En
los átomos, los electrones están distribuidos en niveles de energía
estacionaria o fija.
Los
electrones se mueven alrededor del núcleo sin perder ni ganar energía y sólo lo
hacen cuando pasan de un nivel a otro.
Un
nivel de energía está formado por igual número de subniveles.
Un
subnivel de energía consta de uno o más orbitales o nubes electrónicas.
Un
orbital o nube electrónica se llena con dos electrones con rotación contraria,
es decir, distinto número de spin (número cuántico s).
Gracias
a estos autores ahora actualmente conocemos a mayor medid el modelo atómico
junto a eso que serian los átomos neutrones y protones que a gran tamaños nos
están ayudando a comprender mayormente la formación de moléculas y a entender
con facilidad curas, m o bien enfermedades que en un principio eran imposibles
de resolver.
Estos
serian los modelos atómicos que actualmente se conocen, muchas gracias si es
que te quedaste a leer todo espero y sea un tema que te allá parecido muy
interesante, al igual que te ayude con investigaciones o bien te de un mejor
panorama de los modelos atómicos.
A continuación
te dejare un vídeo, para el mayo entendimiento del tema y sea un poco más didáctico
aprender sobre los modelos atómicos:
Bibliográficas:
Otero Pedro Víctor Yahir NL.
25 1°E