Configuración electrónica y números cuánticos
Antes que nada hay que saber de donde vienen los números cuánticos junto con la configuración electrónicaSi bien esto es parte de la química hoy en día, los números cuánticos fueron una propuesta de Scrondinger en su modelo atómico que fue considerado como el quinto y estas radican en describir las características de todos los electrones de un átomo, que nos permitirá ver la posición y la energía del electrón. Por esta información esperamos que les ayude a comprender mejor este tema y al igual les ayude a obtener una mayor información o conocimiento de este tema.
Como están formados los números cuánticos
Seguramente te estarás preguntando que son los números cuánticos, el cual habla todas las características de los electrones de un átomo y para ello utilizó los números cuánticos.
Los números cuánticos nos indican la posición y la energía
del electrón, estos se representan por las letras:
n: el número cuántico principal, nos indica el nivel de
energía donde se encuentra el electrón.
l: número cuántico secundario, este nos indica el orbital en
el que se encuentra el electrón.
m: número cuántico magnético, este representa la orientación
de los orbitales.
s: número cuántico spin, nos describe la orientación en la
que gira el electrón.


Estos números cuánticos son frecuentemente utilizados en la
configuración electrónica en química. Pero te preguntaras que es la configuración electrónica, bueno te daremos una breve explicación de este:
La configuración electrónica es el modo en el cual los
electrones están ordenados en un átomo. Como los electrones son fermiones están
sujetos al principio de exclusión de Pauli, que dice que dos fermiones no
pueden estar en el mismo estado cuántico a la vez. Por lo tanto, en el momento
en que un estado es ocupado por un electrón, el siguiente electrón debe ocupar
un estado mecano cuántico diferente.
Para poder obtener una configuración de electrónica debe uno bazar en el diagrama de la configuración de electrónica cual se basan en 1s, 2p, 3d, 4f los cuales forman un diagrama el cuales te presentamos a continuación:
Para poder obtener una configuración de electrónica debe uno bazar en el diagrama de la configuración de electrónica cual se basan en 1s, 2p, 3d, 4f los cuales forman un diagrama el cuales te presentamos a continuación:
este diagrama es indispensable para la configuración electrónica, una regla que uno siempre se debe acordar cuando se hace un configuración electronica es que el conteo del lado derecho para terminar en el extremo izquierdo por diagonal.
Al igual sucede con los numero cuánticos pues depende de factores para saber su valor.
n: depende de del ultimo numero colocado en el diagrama
l: depende de la ultima letra colocada en el diagrama por ejemplo s, px, pz entre otros
m: depende de la ultima localización de la flecha (-3, -2, -1, 0, 1, 2, 3) para darle su valor numérico.
s: depende de la posición de la flecha que concluye el diagrama (+1/2, -1/2) ya sea arriba(+) abajo (-)
esto en general son las reglas para obtener tanto el diagrama como los números cuánticos
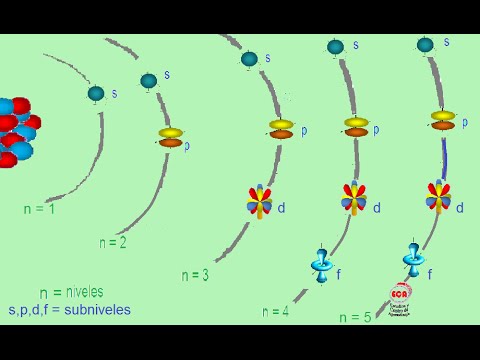

Aquí les dejamos un link de un video para que puedan entender mejor este tema
esperemos y les guste y les facilite en sus actividades
En conclusión se puede decir que se trata sobre los números cuánticos así como cuantos hay y quienes fueron sus autores. Tomando en cuenta que todo tiene que ver mucho con la configuración, ya que está emplea el modelo atómico de Schrodinger el cual pone en efecto los números cuánticos para poder realizar la configuración cuya función indica la manera en la cual todos los electrones se estructuran, comunican u organizan en un atomo. La configuración es importante ya que determina las propiedades todos combinacion química y por lo tanto su posicion en la tabla periodica de los elementos
conclusiones personales
VictorY Otero:
En general todos tenemos poco conocimiento la química, no obstante este tema trata de mostrar con mayor claridad los puntos de la configuración electrónica y los números cuánticos; en cuanto a las leyes de cada punto es una herramienta indispensable para todos los que quieran estudiar química, es posible que este información ayuda algunos de mis compañeros de 3° secundaria y 1° de bachiller, no obstante también ayude a las nuevas generaciones como apoyo a la clase de química en especial el tema del finalizado, agradezco a los que se quedaron el final de la lectura.
PabloA.gutierrez:
En conclusión creo
que es uno de los temas mas importante de la química ya que nos
explica a todos como saber la carga de un electrón y
su posición en la que esta , puesto que a algunos se les hace complicado este tipo de temas porque son
muy complejos al ver la cantidad de cosas que hay en estos temas en las que
vemos muchos procedimientos extraños y difíciles para resolver una cosa tan
pequeña como algunos átomos
Amando Mastranzo:
En conclusión los números cuánticos nos tratan explicar cómo y para qué utilizarlos ya que algunas personas no saben que son o cuál es la función de cada uno de cada uno de ellos ya que no es un tema del todo sencillo. Aquí les vamos a mostrar y explicar este tema, cada número y sus especificaciones tal y como son no tenga ninguna otra duda y les ayude en sus tareas o investigaciones ya que este es uno de todo los temas fundamentales en la materia de químicaAmando Mastranzo:
MaxMusic:
En conclusión se puede ver que este tema es de suma importancia para la química cuántica aparte de ser muy interesante llegaron a ser determinante para lograr describir la naturaleza ondulatoria de un átomo y resulta mucho más eficaz tratar a los electrones en los átomos como ondas ya que están asociadas a algunas magnitudes físicas y sistemas cuanticos. No obstante Tratamos de explicar claridad el tema para ayudar a algunos jóvenes a aprender más sobre este ya que a muchas no a todos se les dificulta
referencias:
http://iiquimica.blogspot.com/2006/03/configuracin-electrnica.html
http://significadodelosnumeros.com/significado-numeros-cuanticos/
https://www.aev.cgfie.ipn.mx/Materia_quimica/temas/tema2/subtema4/subtema4.html
autores:
Otero Pedro Victor Yahir NL.25 1°E
Gutierrez Piedras Pablo Antonio NL.12 1°E
Nava Manzano José Máx NL.24 1°E
Mastranzo Juárez Amando NL.17 1°E

No hay comentarios.:
Publicar un comentario